Novo exame de sangue para Câncer Colorretal: O Que a ciência já sabe e o que ainda precisamos discutir

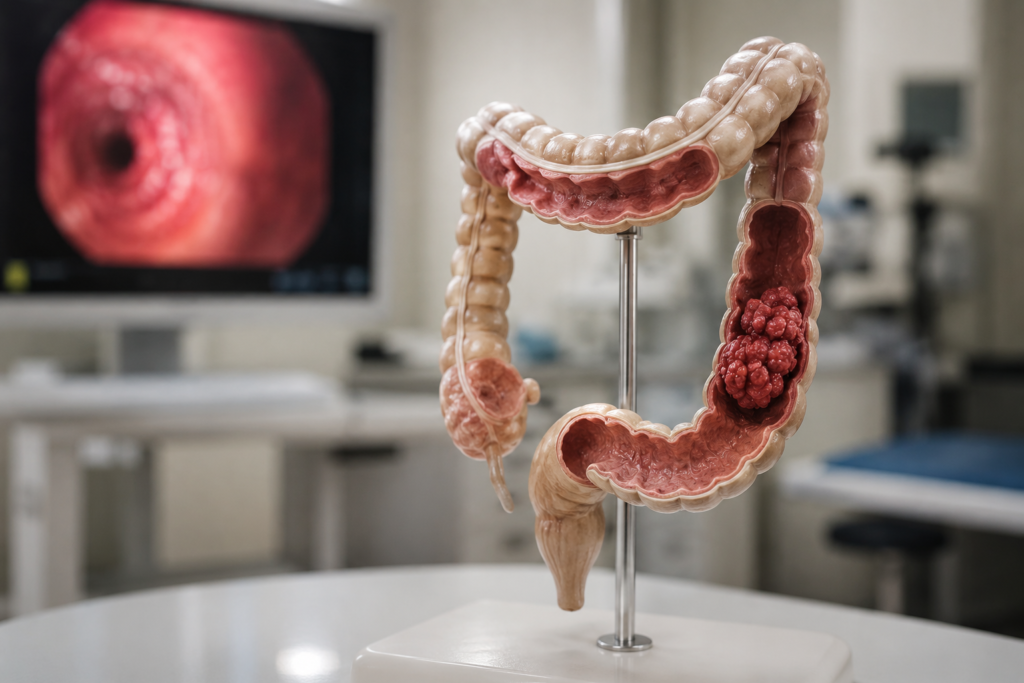
Como já discutimos em outras publicações: o câncer colorretal é o segundo tipo de tumor maligno mais diagnosticado no Brasil, e uma de suas características mais preocupantes é a tendência de ser detectado tardiamente. De acordo com o Instituto Nacional de Câncer (INCA), estima-se que mais de 45 mil novos casos sejam diagnosticados anualmente no país. E a maioria deles, infelizmente, em estágios avançados, quando as chances de cura já são significativamente menores. É nesse contexto que uma novidade científica ganhou destaque mundial em 2024: a aprovação, pela Food and Drug Administration (FDA) dos Estados Unidos, do primeiro exame de sangue para rastreamento do câncer colorretal em pacientes de risco médio. O teste, chamado Shield, foi desenvolvido pela empresa Guardant Health e representa uma mudança relevante na forma como pensamos o diagnóstico precoce desse tumor. Mas, como toda inovação na Medicina, ele precisa ser compreendido com rigor e critério clínico. O que é o exame de sangue Shield para Câncer Colorretal? O Shield é um exame baseado na detecção de DNA tumoral circulante livre (ctDNA) no sangue — fragmentos de material genético liberados por células cancerosas na corrente sanguínea —, além de proteínas associadas ao tumor colorretal. Trata-se do conceito de biópsia líquida aplicado ao rastreamento populacional. Diferentemente da colonoscopia, que exige preparo intestinal, sedação e uma estrutura hospitalar específica, o Shield é realizado com uma simples coleta de sangue em uma consulta de rotina. O material é então enviado a um laboratório especializado para análise. O exame estava disponível nos Estados Unidos por prescrição médica desde 2022 como teste laboratorial desenvolvido. Em julho de 2024, recebeu a aprovação formal da FDA como método de rastreamento primário para indivíduos a partir de 45 anos com risco médio para câncer colorretal; tornando-se o primeiro exame sanguíneo a obter essa classificação regulatória no país. O que diz o Estudo ECLIPSE — a base científica do Shield A aprovação da FDA foi fundamentada nos resultados do estudo clínico ECLIPSE (Evaluation of ctDNA LUNAR Assay In an Average Patient Screening Episode), publicado no New England Journal of Medicine em março de 2024. Trata-se de um dos maiores estudos de rastreamento de câncer colorretal já conduzidos: mais de 20.000 participantes recrutados em comunidades rurais e urbanas, em 37 estados americanos, em mais de 200 centros de pesquisa. Os resultados demonstraram que o Shield identificou corretamente 83% das pessoas com câncer colorretal confirmado, com uma especificidade de 90% para neoplasias avançadas. Em comparação, testes de DNA fecal já estabelecidos apresentam sensibilidade ligeiramente superior, entre 88% e 92%. Isso significa que o exame de sangue para câncer colorretal tem desempenho próximo ao dos testes fecais convencionais para detectar o câncer já instalado, o que é clinicamente significativo. O que o exame de sangue para câncer colorretal não detecta — e por que isso importa Aqui reside um ponto de extrema relevância clínica, destacado tanto pelo estudo ECLIPSE quanto pela revisão publicada em junho de 2025 na Nature Reviews Clinical Oncology por McCabe, Mauro e Schoen: o exame Shield apresenta sensibilidade limitada para a detecção de lesões precursoras avançadas (APLs) — os chamados pólipos de alto risco, que precedem o desenvolvimento do câncer. Segundo os dados do próprio fabricante, o teste detecta apenas cerca de 13% dos pólipos avançados. Isso significa que 87% das lesões precursoras significativas passariam despercebidas por esse exame. Esse dado muda completamente a forma de interpretar o Shield. A colonoscopia não é apenas um método de diagnóstico. Ela permite identificar e remover pólipos antes que se tornem cancerosos, funcionando ao mesmo tempo como rastreamento e como prevenção. O exame de sangue, tal como está, não tem essa capacidade. Além disso, aproximadamente 10% dos resultados positivos no Shield são falsos positivos, exigindo uma colonoscopia de confirmação, com todos os custos, desconfortos e riscos associados a esse procedimento. Colonoscopia vs. Exame de Sangue para câncer colorretal: não é uma disputa, É uma complementaridade Uma das perguntas mais frequentes que recebo no consultório da Waken Clínica é: “Dra. Gilmara, com esse novo exame de sangue, ainda preciso fazer colonoscopia?” A resposta é: depende do contexto clínico de cada paciente; e essa avaliação individualizada é insubstituível. A colonoscopia permanece o padrão-ouro para o rastreamento do câncer colorretal. Ela permite: Já o exame de sangue oferece vantagens distintas: O ponto fundamental, bem articulado pelo Dr. Michael Cecchini, oncologista médico da Universidade Yale, é que “o melhor exame de rastreamento é aquele que o paciente está disposto a realizar”. Dito isso, a escolha do método precisa ser orientada pelo médico com base no histórico, nos fatores de risco e nas preferências do indivíduo. O contexto brasileiro: por que isso é relevante para nós? No Brasil, as taxas de adesão ao rastreamento e exame de sangue para câncer colorretal ainda são muito aquém do recomendado. A maioria das diretrizes nacionais e internacionais recomenda o início do rastreamento a partir dos 45 a 50 anos para a população de risco médio, mas uma parcela expressiva dos brasileiros elegíveis nunca realizou qualquer exame de rastreamento. Os motivos são múltiplos: dificuldade de acesso, medo do procedimento, desconhecimento sobre a importância do rastreamento precoce e ausência de sintomas nas fases iniciais da doença. O câncer colorretal é traiçoeiro justamente por isso: na maioria dos casos, só produz sintomas quando já está em estágios avançados. A sobrevida em cinco anos para o câncer colorretal diagnosticado em fase localizada supera 90%. Quando detectado após disseminação a distância, esse número cai para cerca de 15%. O rastreamento precoce salva vidas — essa é a premissa que não muda. Nesse sentido, a existência de uma alternativa como o exame de sangue tem potencial de ampliar o alcance do rastreamento para grupos que, por diversas razões, resistem à colonoscopia. Isso já foi demonstrado em estudos controlados, nos quais pacientes que haviam recusado tanto a colonoscopia quanto o exame de fezes aceitaram realizar o exame sanguíneo, triplicando as taxas de rastreamento nesse grupo específico. O que diz a evidência mais recente da Nature Reviews Clinical Oncology A revisão publicada em
Bactérias Intestinais e Câncer Colorretal em Jovens: O que um estudo histórico na Nature acabou de revelar
Uma das perguntas que mais me inquietam como Coloproctologista, e que também preocupa crescentemente a comunidade científica global, é: por que o câncer colorretal está aumentando em adultos jovens? Por décadas, esse tumor foi tratado como doença de pessoas acima dos 60 ou 70 anos. Hoje, esse perfil mudou de forma alarmante. Nos últimos 20 anos, a incidência de câncer colorretal em pessoas com menos de 50 anos dobrou em diversos países. Nos Estados Unidos, já representa um em cada cinco novos diagnósticos da doença — um aumento de 11% nessa faixa etária em duas décadas. No Brasil, os dados do INCA apontam tendência semelhante, com diagnósticos cada vez mais frequentes em adultos entre 30 e 49 anos. E o pior: muitos chegam já em estágio avançado, justamente porque nem os próprios pacientes nem os profissionais de saúde associam sintomas como sangramento retal ou dor abdominal persistente a câncer em pessoas jovens. Agora, um estudo publicado em abril de 2025 na revista Nature, o periódico científico mais influente do mundo, oferece uma das respostas mais concretas e perturbadoras que já tivemos para essa questão: uma toxina produzida por bactérias intestinais comuns, chamada colibactina, pode estar deixando uma “marca genética” permanente no intestino de crianças, acelerando em décadas o desenvolvimento do câncer colorretal. A pesquisa, liderada pelo professor Ludmil Alexandrov da Universidade da Califórnia em San Diego e coordenada internacionalmente pela Agência Internacional de Pesquisa em Câncer (IARC/OMS), analisou o sequenciamento completo do genoma de 981 tumores colorretais de pacientes em 11 países de 4 continentes, dentro do projeto Mutographs Cancer Grand Challenge. O Brasil foi um dos países participantes, com pesquisadores brasileiros entre os autores do estudo — profissionais do A.C.Camargo Cancer Center e da Universidade Federal do Rio Grande do Sul, além de pesquisadores ligados ao Hospital de Amor (Barretos) e à PUCRS. O objetivo inicial era entender porque as taxas de câncer colorretal variam tanto entre diferentes países e regiões do mundo. O que os pesquisadores encontraram, entretanto, foi muito além disso; e mudou a forma como entendemos o câncer colorretal de início precoce. A colibactina é uma genotoxina. Isto é, uma substância capaz de causar danos diretamente ao DNA das células. Ela é produzida por cepas de Escherichia coli e outras bactérias que carregam uma região específica do genoma bacteriano chamada ilha de patogenicidade pks. Essas bactérias habitam naturalmente o intestino humano. Estimativas indicam que 20 a 30% da população abriga cepas produtoras de colibactina no microbioma intestinal; e a maioria das pessoas não sabe disso, pois não provoca sintomas diretos. O mecanismo de dano é sutil e acumulativo: ao colonizar o epitélio do cólon, essas bactérias produzem colibactina, que ataca o DNA das células do revestimento intestinal e gera mutações características — as chamadas “assinaturas mutacionais” SBS88 e ID18. O estudo da Nature utilizou sequenciamento completo do genoma para identificar essas assinaturas nos tumores dos pacientes. Assim como a fumaça do cigarro deixa um padrão específico de mutações no pulmão de quem fuma, a colibactina deixa uma impressão genética única no cólon; e essa impressão foi encontrada em proporção muito maior nos tumores de pacientes jovens. A descoberta mais impactante do estudo é sobre o momento em que essas mutações são geradas. A análise do “registro arqueológico” do DNA tumoral, que permite estimar quando determinadas mutações ocorreram ao longo da vida de um indivíduo, indicou que a exposição à colibactina acontece predominantemente antes dos 10 anos de idade. É no intestino da criança que a toxina atua com maior força, deixando marcas genéticas que permanecerão nas células por toda a vida. Esse “golpe precoce” no DNA intestinal parece colocar o organismo de 20 a 30 anos à frente no processo de carcinogênese. Em vez de desenvolver câncer colorretal aos 65 ou 70 anos, que seria o curso esperado para alguém com mutações acumuladas ao longo da vida, essas pessoas chegam ao tumor já aos 35 ou 45 anos. Os dados são contundentes: as assinaturas colibactina (SBS88 e ID18) foram encontradas 3,3 vezes mais frequentemente em pacientes diagnosticados com câncer colorretal antes dos 40 anos do que naqueles diagnosticados após os 70. E quanto mais jovem o paciente ao diagnóstico, maior a prevalência dessas assinaturas. Além disso, o estudo mostrou que a colibactina atua como um evento precoce no desenvolvimento do tumor: as mutações por ela induzidas se encontram predominantemente nas células fundadoras do câncer, e não nas células que surgem posteriormente durante a progressão tumoral. Isso confirma que a exposição à toxina precede e, possivelmente, impulsiona todo o processo de carcinogênese. Um dos mecanismos pelo qual a colibactina pode contribuir para o desenvolvimento do câncer colorretal envolve o gene APC (adenomatous polyposis coli), um dos principais genes supressores tumorais do cólon. Mutações no APC são um dos eventos mais precoces e característicos no desenvolvimento do câncer colorretal. O estudo demonstrou que a assinatura mutacional ID18, gerada pela colibactina, é responsável por aproximadamente 25% das mutações de inserção/deleção no gene APC em pacientes colibactina-positivos. Como as mutações no APC ocorrem tipicamente no início da cadeia de alterações genéticas que leva ao câncer colorretal, um “primeiro acerto” nesse gene durante a infância pode dar ao organismo décadas de vantagem no desenvolvimento tumoral, e resultar em câncer em idades muito mais jovens. O estudo revelou também que as assinaturas de colibactina são mais prevalentes em países com maiores taxas de incidência de câncer colorretal; e especialmente em países com maior incidência de câncer colorretal de início precoce. Essa correlação foi estatisticamente significativa e independente de outros fatores analisados. Os países estudados foram divididos entre aqueles com incidência intermediária, incluindo Brasil, Colômbia, Irã e Tailândia; e países de alta incidência, como Argentina, Canadá, Rússia, Sérvia, República Tcheca, Polônia e Japão (com a maior taxa de incidência padronizada por idade do grupo, de 37 por 100.000 habitantes). O que torna esse dado especialmente relevante para nós, no Brasil, é que nosso país integrou a coorte do estudo. Isso significa que as descobertas têm aplicabilidade direta para o contexto clínico e
Cirurgião oncológico: o que faz, quando procurar e qual a diferença para o oncologista clínico

Quando um paciente ouve a palavra “câncer”, quase sempre o pensamento corre mais rápido que a compreensão. Surgem medo, insegurança e a urgência de fazer algo imediatamente. Mas, em oncologia, agir rápido é importante, e agir certo é indispensável. Nem todo tumor será tratado da mesma forma. Nem toda cirurgia deve ser feita de imediato. Nem todo caso começa com quimioterapia. É justamente nesse ponto que entra a importância do cirurgião oncológico: um especialista treinado para avaliar o tumor com lógica oncológica, respeitando diagnóstico, estágio da doença, possibilidade de cura, controle local e integração com toda a equipe de tratamento. No Brasil, a relevância desse tema é evidente. O INCA estima 781 mil casos novos de câncer por ano no triênio 2026–2028; excluindo o câncer de pele não melanoma, são cerca de 518 mil novos casos anuais. Entre os mais frequentes estão mama, próstata, cólon e reto, pulmão e estômago, doenças em que a cirurgia frequentemente participa do diagnóstico, do estadiamento ou do tratamento. O que é cirurgia oncológica A cirurgia oncológica é a área da Medicina dedicada ao tratamento cirúrgico dos tumores. Segundo o INCA, ela consiste na retirada do tumor por meio de operações no corpo do paciente e, quando indicada, tem como objetivo remover completamente a doença visível. Mas o seu papel vai muito além de “tirar o tumor”. A cirurgia também pode ser fundamental para confirmar o diagnóstico por biópsia, definir a extensão da doença, tratar complicações, controlar sintomas e, em alguns casos, integrar-se a quimioterapia, radioterapia, terapia-alvo ou imunoterapia, de forma planejada. Em outras palavras, o cirurgião oncológico não é apenas um cirurgião que opera pacientes com câncer de forma eventual. Trata-se de um profissional com treinamento específico para lidar com princípios oncológicos essenciais: margens cirúrgicas adequadas, manipulação segura do tumor, avaliação linfonodal, integração com o estadiamento, indicação correta do momento da cirurgia e articulação com a equipe multidisciplinar. O próprio NCI define o surgical oncologist como o cirurgião com treinamento especial para realizar biópsias e outros procedimentos cirúrgicos em pacientes com câncer. Nem todo tumor é câncer, mas nem todo tumor benigno é irrelevante Um ponto importante, abordado no vídeo, é que “oncologia” não significa apenas câncer avançado nem se resume a uma sentença grave. Em Medicina, tumor significa, de forma ampla, um crescimento anormal de tecido. Esse tumor pode ser benigno ou maligno. O tumor maligno é o câncer. Já o benigno não costuma ter comportamento invasivo ou metastático como o câncer, mas isso não significa que seja sempre inofensivo. Dependendo do local, do tamanho e do efeito compressivo sobre estruturas nobres, até tumores benignos podem provocar complicações importantes e, em situações específicas, risco de vida. Esse esclarecimento é valioso porque ajuda a reduzir dois extremos muito comuns: o pânico diante de qualquer “nódulo” e, no lado oposto, a banalização de lesões que “parecem benignas” sem avaliação adequada. O caminho seguro é sempre o diagnóstico preciso, com exame clínico, imagem quando necessário, discussão especializada e, em alguns casos, biópsia. Qual a diferença entre oncologista clínico e cirurgião oncológico Essa é, talvez, a dúvida mais frequente entre pacientes e familiares. O oncologista clínico é o médico que atua principalmente com tratamentos sistêmicos, como quimioterapia, hormonioterapia, imunoterapia e terapias-alvo. Ele acompanha o comportamento biológico da doença, avalia risco de recorrência, resposta aos tratamentos e necessidade de medicações antes ou depois da cirurgia. Já o cirurgião oncológico é o especialista no manejo cirúrgico dos tumores, atuando no diagnóstico, no estadiamento, na ressecção oncológica e, quando necessário, em procedimentos paliativos ou reconstrutivos integrados ao tratamento. Esses profissionais não competem entre si. Eles se complementam. Em muitos casos, o melhor resultado depende justamente da sequência correta entre as etapas. Há tumores em que a cirurgia vem primeiro. Em outros, o ideal é iniciar com tratamento sistêmico ou radioterapia e operar depois. Em alguns cenários, a cirurgia pode nem ser a primeira escolha. Por isso, as diretrizes modernas enfatizam que o plano terapêutico deve ser definido antes de qualquer tratamento não emergencial, dentro de discussão multidisciplinar. Por que a avaliação multidisciplinar faz tanta diferença O tratamento oncológico evoluiu muito justamente porque deixou de ser uma decisão isolada. Hoje, câncer bem tratado é, idealmente, câncer discutido por equipe. Tumor boards e reuniões multidisciplinares ajudam a revisar diagnóstico, estadiamento, sequência terapêutica, necessidade de exames adicionais e indicação do melhor tipo de cirurgia para cada caso. Uma revisão sistemática e meta-análise publicada em 2025 mostrou que a discussão multidisciplinar pode alterar condutas e se associar a melhores desfechos em pacientes com câncer. Outras revisões recentes reforçam que esse modelo tende a melhorar a personalização do cuidado e a consistência das decisões clínicas. Na prática, isso significa algo muito importante para o paciente: não basta operar; é preciso operar a pessoa certa, no momento certo, com a estratégia certa. Em oncologia, o detalhe técnico importa. A extensão da ressecção, o planejamento das margens, a avaliação dos linfonodos, a via de acesso e a integração com tratamentos complementares influenciam diretamente prognóstico, risco de recorrência, complicações e qualidade de vida. O que o cirurgião oncológico faz na prática O papel do cirurgião oncológico pode começar muito antes da cirurgia definitiva. Em alguns casos, ele participa da investigação por meio de biópsias incisionais, excisionais ou procedimentos minimamente invasivos para esclarecer a natureza de uma lesão. Em outros, ele atua no estadiamento cirúrgico, ajudando a determinar a real extensão da doença. E, evidentemente, tem papel central no tratamento curativo de muitos tumores sólidos, quando a retirada completa da lesão é possível e indicada. Além disso, há situações em que a cirurgia é indicada para aliviar sintomas ou tratar complicações, mesmo quando a cura não é o objetivo principal. Obstruções, sangramentos, perfurações, dor refratária ou massas tumorais que comprometem funções vitais podem exigir abordagem cirúrgica em contexto paliativo. Isso também é oncologia de qualidade: oferecer benefício real, com indicação criteriosa, foco em controle de sintomas e respeito aos objetivos do paciente. Quando procurar um cirurgião oncológico De forma objetiva, algumas situações costumam justificar avaliação com cirurgião oncológico:

